首款创新型生物药抗PD-1抗体批准上市 为黑色素瘤患者带来新选择
作者:admin 日期:2023-11-21 12:04:58 浏览:87 分类:资讯
9月29日,乐普生物(2157.HK)披露公告称,公司旗下首款创新型生物药抗PD-1抗体——普佑恒™(普特利单抗注射液)已获得中国国家药品监督管理局(NMPA)批准上市。这是继今年7月MSI-H/
9月29日,乐普生物(2157.HK)披露公告称,公司旗下首款创新型生物药抗PD-1抗体——普佑恒(普特利单抗注射液)已获得中国国家药品监督管理局(NMPA)批准上市。这是继今年7月MSI-H/dMMR实体瘤获批上市后,普佑恒(普特利单抗注射液)获批的又一适应症。
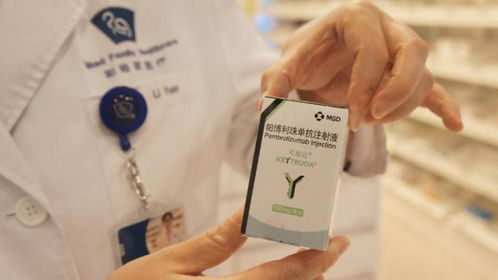
公开资料显示,乐普生物于2021年6月向NMPA提交了普特利单抗用于黑色素瘤适应症的上市申请,并获得受理。本次普特利单抗的获批,将为中国黑色素瘤患者带来免疫治疗的新选择。
黑色素瘤是一种来源于黑色素细胞的恶性肿瘤,常见于皮肤,亦见于黏膜、眼脉络膜等部位。由于死亡率高、转移率高、治疗难度大,其素有"癌中之王"之称。目前,黑色素瘤早期患者大多采用手术切除治疗,中晚期治疗手段则非常有限。
相关数据显示,全球每年新发黑色素瘤病例16万例,死亡48000例。目前,我国黑色素瘤发病人数平均每年增长6.1%。早期黑色素瘤5年生存率约为50%-90%,晚期黑色素瘤5年生存率不足10%。
普佑恒(普特利单抗注射液)适用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤适应症患者。据了解,普特利单抗获批主要基于一项单臂、开放、关键性II期临床研究,该试验主要终点是由独立影像学数据委员会(IRC)根据 RECIST 1.1 标准评估的客观缓解率(ORR)。该次试验共入组119名患者,截至2021年7月30日,经IRC评估的ORR为20.2%(95%CI:13.4-28.5,1例完全缓解,23例部分缓解)。
研究结果表明,普佑恒治疗既往接受全身系统治疗失败的不可切除或转移性黑色素瘤达到预设主要终点标准,具有良好安全性。该项临床研究结果于2021年美国临床肿瘤学会(ASCO)年会上首次公布。
据了解,普佑恒(普特利单抗注射液)通过阻断PD-1与其配体PD-L1及PD-L2的结合来恢复免疫细胞杀死癌细胞的能力,其创新性地采用抗体工程技术,可大幅延长患者半衰期。与已上市或进入III期临床试验所有抗PD-1抗体相比,普佑恒(普特利单抗注射液)半衰期均值为21.8(单次给药)及38.2天(稳态)。
除了黑色素瘤,围绕普佑恒乐普生物正在加速推进在多个实体瘤上的开发并积极展开肿瘤免疫联合疗法,包括胃癌、肝癌、肺癌等高发癌种的治疗。目前,乐普生物正在推进普佑恒TM与伊立替康联合用于胃癌二线治疗的III期注册性临床研究。
如果想实时了解更多理财新闻,欢迎关注理财笔记网。
猜你还喜欢
- 11-21 医药产品介绍:申万菱信中证申万医药生物
- 11-21 华宝兴业医药生物优选基金(240020)
- 11-21 医药板块的投资怎么做?医疗板块和医药生物板块是同一类吗?
- 11-21 SpaceX获FAA许可,“星舰”即将第二次发射,马斯克的“火星梦”再启程
- 11-21 PIMCO首席警告:通胀未解,债券市场过度乐观
- 11-21 巴菲特最新调仓曝光:第三季度清仓7股,减持多只股票
- 11-21 公众号“抢跑”致股价提前涨停?汇纳科技收到深交所关注函
- 11-21 大消息 多股涨停!锂矿板块强劲反弹 汽车产业链震荡走高
- 11-21 实探小米汽车生产基地:已实现小批量试生产 三年要卖90万辆
- 11-21 广电总局将再次开展为期1个月的网络微短剧专项整治工作
- 11-21 Q3美股13F追踪:王亚伟增持AI概念股 高毅减持拼多多景林仍坚守
- 11-21 华为又“上新”!余承东:问界M9将亮相广州车展
取消回复欢迎 你 发表评论:
- 最近发表
- 标签列表
- 友情链接
暂无评论,来添加一个吧。